Tocris Bioscience 社 標的タンパク質分解ツール Active Degrader(PROTAC)


Tocris Bioscience 社(以下 Tocris 社)より販売されている Active Degrader(PROTAC)は、細胞内の標的タンパク質をノックダウンするための新しい技術を基盤とした製品です。ここでは、がん研究の分野で注目を集めつつある本製品の特長について解説します。
- 利便性:低分子で細胞膜透過性があるため、トランスフェクションや発現ベクターを必要とせず、培地に添加するだけで細胞内に容易に取り込まれます。
- さまざまな細胞への汎用性:トランスフェクションが困難な細胞も含め、さまざまな細胞に対して使用することができます。
- 調節可能な持続時間:ウォッシュアウトによって投与前の状態に戻すことができるため、効果の持続時間を調整可能です。
- 少量での効果発揮:UPS は触媒作用のため、化学量論以下の濃度で使用可能です。
製品説明
構造と作用機序
Active Degrader は、①標的タンパク質に対するリガンドと、③E3 リガーゼに対するリガンドを、②クロスリンカーでつないだ構造です(図 1)。
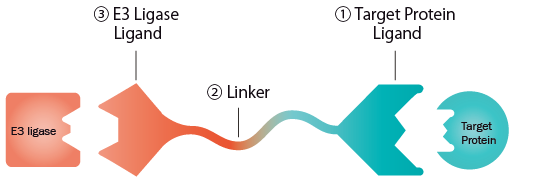
図 1 Active Degrader の構造
Active Degrader が、E3 リガーゼと目的タンパク質をつなぎ合わせることによって、目的タンパク質をポリユビキチン化し、プロテアソームによる消化を経て、ペプチド断片にまで分解します(図 2)。
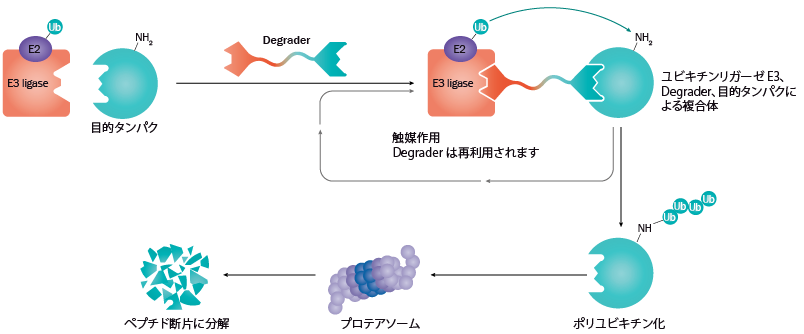
図 2 Active Degrader の作用機序
Adapted from Tinworth et al. MedChemComm. 2016, 7, p.2206-2216.
関連資料

最新情報は Tocris Bioscience 社 の Web site(PROTAC Degraders & Targeted Protein Degradation)をご参照ください。
ビデオセミナー:低分子化合物による細胞内タンパク質発現調節
~ 細胞内タンパク質分解システムについて ~
PROTAC(PROteolysis TArgetting Chimera)などの Targeted Protein Degradation(標的タンパク質分解)技術は、ユビキチン-プロテアソーム システム(UPS)を利用して細胞内の標的タンパク質を分解するシステムです。標的タンパク質と E3 リガーゼをキメラ低分子化合物を使って人為的に引き合わせることで、標的タンパク質をユビキチン化します。ユビキチン化された標的タンパク質はプロテアソームによりペプチド断片に分解され、薬理作用が発現します。
従来の低分子阻害剤では制御が困難であった、酵素活性を持たないタンパク質を標的に出来るだけでなく、阻害剤とは異なる薬理作用が発見される可能性もあります。
PROTAC(PROteolysis TArgetting Chimera)は Arvinas Operations 社の商標であり、Tocris Bioscience 社の Degrader はライセンス下で製造販売しています。
価格表
がん研究で有用な Active Degrader とその機能
現在販売している Active Degrader のうち、特にがん研究で有用と思われる製品と、それぞれの機能について例を示します。
がん研究に有用な製品例
| 化合物名 | メーカー 製品番号 |
容量 | 目的タンパク質 | 特長 |
|---|---|---|---|---|
| MZ 1 | 6154 | 5 mg | BRD4 | BRD2 および BRD3 よりも BRD4 を選択的に分解します。AML 細胞株で強力な抗増殖および細胞毒性効果を示します。* |
| dBET1 | 6327 | 5 mg | BET Bromodomains | in vitro で癌細胞株の BET ブロモドメインを枯渇させ、ヒト AML 異種移植片を有するマウスで in vivo で MYC をダウンレギュレーションします。** |
| AT 1 | 6356 | 5 mg | BRD4 | BRD2 と BRD3 への作用はごくわずかで、BRD4 を選択的に分解します。最も選択的な BRD4 Degrader です。* |
| CM 11 | 6416 | 5 mg | pVHL30 | ロングフォームの VHL である pVHL30* において、自己分解を可能としたホモ型の PROTAC です。 |
| TL 12-186 | 6524 | 5 mg | Multikinase | in vitro において種々のキナーゼを分解します。** |
| THAL SNS 032 | 6532 | 5 mg | Cdk9 | Cdk9 を強力かつ選択的に分解します。** |
| dTAG 13 | 6605 | 5 mg | FKBP12F36V fusion proteins | 変異型 FKBP12F36V 融合タンパクを分解します。ターゲットの検証を行う上での遺伝的方法に代わる方法です。 |
| dBRD9 | 6606 | 5 mg | BRD9 | BRD9 を強力かつ選択的に分解します。** |
| dTRIM 24 | 6607 | 5 mg | TRIM24 | TRIM24 を分解します。MOLM-13 cells において抗増殖性を示します。** |
| TL 13-12 | 6744 | 5 mg | Anaplastic lymphoma kinase (ALK) | 選択的な ALK の Degrader。ALK 陽性がん細胞の増殖を抑制します。TL 13-112 (#6745) と比較して、Aurora A キナーゼよりも ALK に対して高い選択性を示します。** |
| TL 13-112 | 6745 | 5 mg | ALK | 選択的な ALK の Degrader。ALK 陽性がん細胞の増殖を抑制します。 ** |
| dTAG-7 | 6912 | 5 mg | FKBP12F36V fusion proteins | 変異型 FKBP12F36V 融合タンパクを分解します。ターゲットの検証を行う上での遺伝的方法に代わる方法です。** |
| BSJ-03-123 | 6921 | 5 mg | Cdk6 | 選択的な Cdk6 の Degrader。密接に関連している Cdk4 を分解することなく、Cdk6 のみを分解します。** |
| VZ 185 | 6936 | 5 mg | BRD7/9 | 強力かつ選択的な BRD7/9 の Degrader。EOL-1、A-204 がん細胞に対して細胞毒性を示します。* |
| BSJ-04-132 | 6937 | 5 mg | Cdk4 | 選択的な Cdk4 の Degrader。Molt-4 cells において Cdk4 を分解する際は、Cdk6 の影響を受けません。** |
| BSJ-03-204 | 6938 | 5 mg | Cdk4/Cdk6 | 選択的な Cdk4/6 の Degrader で、細胞周期を G1 で止め、マントル細胞リンパ腫の細胞増殖を抑制します。** |
| CRBN-6-5-5-VHL | 6948 | 5 mg | Cereblon | 強力かつ選択的な cereblon の Degrader で、細胞膜透過性があります。 |
| aTAG 2139 | 6970 | 5 mg | MTH1 fusion proteins | 強力かつ選択的な MTH1 融合タンパクの Degrader で、in vitro でも in vivo でも使えます。 |
| aTAG 4531 | 6971 | 5 mg | MTH1 fusion proteins | 強力かつ選択的な MTH1 融合タンパクの Degrader で、in vitro でも in vivo でも使えます。 |
| NR 7h | 7177 | 5 mg | p38α/β | 強力かつ選択的な p38α と p38β の Degrader で、in vitro でも in vivo でも使えます。 |
* ダンディー大学からのライセンスに基づいて販売しています。
** ダナ・ファーバー癌研究所からのライセンスに基づいて販売しています。
製品ラインアップは絶賛拡充中です。詳細は Web site をご参照ください。
※掲載内容は 2022 年 5 月現在の情報に基づいています。
