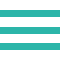国内研究者使用例
Plasmocin™によるマイコプラズマ汚染の検証
マイコプラズマは、自己増殖能を持つ細菌の1/10程度の大きさの微生物で、培養細胞を汚染しやすく細胞と共存して増殖します。細胞培養時の問題は、マイコプラズマに汚染されていても培地が濁ることがありませんので混入に気付きにくい点です。また、マイコプラズマ汚染が研究に及ぼす影響は多大であり、サイトカインの発現異常、染色体の異常、細胞死などを引き起こします。日本組織培養学会細胞バンク委員会とJCRB細胞バンクの調査によると、1500検体程度の解析を実施したところ、平均汚染率は22.4%という結果が報告されており、マイコプラズマ汚染の検査および除去・予防が重要な課題となってきています。
培養細胞研究資源のマイコプラズマ汚染調査 Tiss. Cult. Res. Commun. 26: 159-163 (2007)より引用
データご提供:(独)医薬基盤研究所・生物資源研究部・細胞資源研究室
小澤 裕 研究員 小原 有弘 研究員
実験概要
培養細胞のマイコプラズマ汚染頻度は非常に高く、細胞バンクに寄託される細胞の約18%に汚染が認められる。細胞の性状等に変化を与えない、確実なマイコプラズマの除染は細胞バンクにとって重要な課題である。今回、細胞バンクで第一選択薬として使用しているA社マイコプラズマ除去試薬によって汚染除去できなかった細胞に対して、InvivoGen社 Plasmocin™処理による汚染除去を検証した。
| 年 | 登録数 | 汚染数 | % |
|---|---|---|---|
| 2002 | 34 | 2 | 5.9 |
| 2003 | 40 | 3 | 7.5 |
| 2004 | 32 | 19 | 59.4 |
| 2005 | 48 | 8 | 16.7 |
| 2006 | 40 | 6 | 15.0 |
| 2007 | 53 | 6 | 11.3 |
| 合計 | 247 | 44 | 17.8 |
PCR法、DNA間接蛍光染色法による検査
年間40程度の新規登録細胞
年間3,500アンプルの分譲
実験方法
A社試薬によってマイコプラズマ汚染除去が出来なかった食道扁平上皮がん細胞を用いてPlasmocin™による汚染除去を試行した。マイコプラズマ汚染の検査にはMycoAlert™ Mycoplasma Detection Kit、DNA間接蛍光染色法、Nested-PCR法を用いた。
実験結果
| 細胞バンクに寄託された食道扁平上皮がん細胞 | |
|---|---|
| DNA間接蛍光染色法 | Nested-PCR法 |
 |
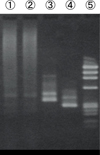 |
| A社マイコプラズマ除去試薬 処理後3ヶ月継続培養した細胞 | |
 |
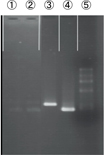 |
| Plasmocin™ 処理後3ヶ月継続培養した細胞 | |
 |
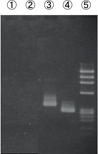 |
①②食道扁平上皮がん ③M. fermentans ④M. orale ⑤マーカー
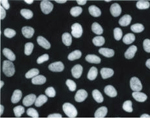
●DNA間接蛍光染色法
マイコプラズマに汚染されてない細胞は核だけが染色されますが、汚染されている細胞はマイコプラズマのDNAも染色されるため、核以外の部分にも小さな蛍光が見られます。
●Nested-PCR法
マイコプラズマに汚染されていればバンドが確認されます。M.fermentans、M.oraleはポジティブコントロール、マーカーはΦX174/HaeIIIです。
| MycoAlert™ | DNA間接 蛍光染色法 | Nested-PCR法 | |
|---|---|---|---|
| 寄託時の食道扁平上皮がん細胞 | + | + | + |
| A社マイコプラズマ除去試薬処理後 3ヶ月継続培養した細胞 |
+ | + | + |
| Plasmocin™処理後3ヶ月継続培養した細胞 | - | - | - |
寄託された細胞ではPCR産物のバンドが認められ、マイコプラズマに汚染されていることがわかる。寄託された細胞をA社除去試薬で処理したところ、それでもPCR産物のバンドが若干認められるため、A社試薬ではマイコプラズマを完全に除染できていないことがわかる。Plasmocin™で処理した細胞ではPCR産物のバンドが認められない。そのためA社除去試薬で除染できなかったマイコプラズマが、Plasmocin™では除染できたと考えられる。
MycoAlert™は Lonza Groupの商標です。
製品詳細はこちら(製品のページへ移動します)
※記載の内容は、'14年1月現在の情報に基づいております。
※研究者のご所属などの情報は、データご提供時の情報に基づいております。